August 24, 2020

2020年6月29日,新版《化妆品监督管理条例》(以下简称“新条例”)的最终版本已正式颁布,将于2021年1月1日起实施,取代1989年首次发布的现行《化妆品卫生监督条例》。
关键要点
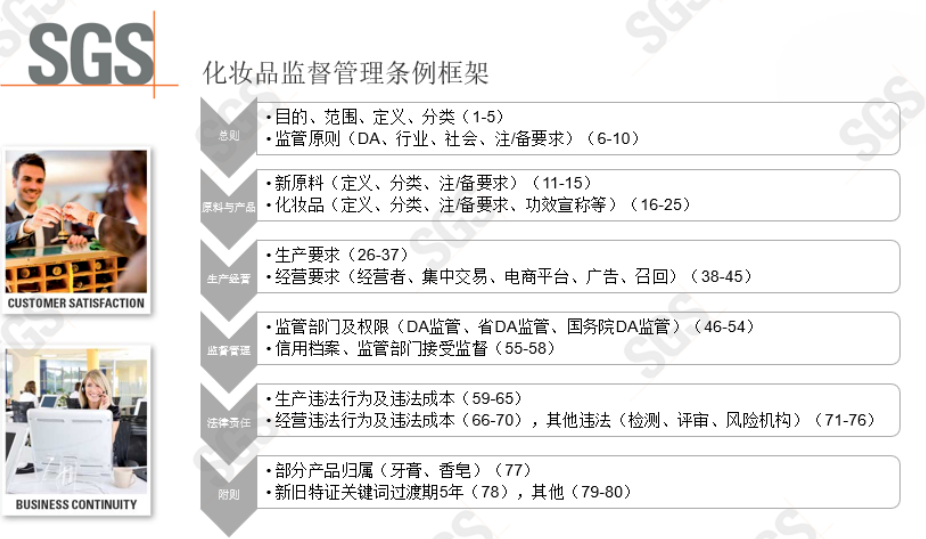
新条例10个关键点,涉及以下5个方面:
化妆品定义
化妆品和化妆品原料分类管理
安全评估和功效宣称
生产经营过程的要求
违法事实及代价
SGS专家针对新条例10个关键点的详细解析:
1、新条例中对化妆品定义:
指以涂擦、喷洒或者其他类似方法,施用于皮肤、毛发、指甲、口唇等人体表面,以清洁、保护、美化、修饰为目的的日用化学工业产品。
2、化妆品分类管理
化妆品分为特殊化妆品和普通化妆品。国家对特殊化妆品实行注册管理,对普通化妆品实行备案管理。
特殊:染发、烫发、祛斑美白、防晒、防脱发、宣称新功效---注册后,才能生产、进口
普通:其他---备案管理(国产:备案后上市;进口:备案后进口)
牙膏参照本条例有关普通化妆品的规定进行管理。牙膏的具体管理办法由国务院药品监督管理部门拟订,报国务院市场监督管理部门审核、发布。香皂不适用本条例,但是宣称具有特殊化妆品功效的适用本条例。
对本条例施行前已经注册的用于育发、脱毛、美乳、健美、除臭的化妆品自本条例施行之日起设置5年的过渡期,过渡期内可以继续生产、进口、销售,过渡期满后不得生产、进口、销售该化妆品。
3、化妆品原料分为新原料和已使用的原料。国家对风险程度较高的化妆品新原料实行注册管理,对其他化妆品新原料实行备案管理。
化妆品新原料:在我国境内首次使用于化妆品的天然或者人工原料为化妆品新原料。
特殊新原料:防腐、防晒、着色、染发、祛斑美白---注册管理
其他新原料:其他---备案管理
新原料转化为已用使用原料过程:
注册人/备案人3年内每年向国务院药监部门报告使用情况与安全性(YES: 纳入已用原料;NO: 撤销注册/取消备案)
申请化妆品新原料注册或者进行化妆品新原料备案,应当提交下列资料:
(一)注册申请人、备案人的名称、地址、联系方式;
(二)新原料研制报告;
(三)新原料的制备工艺、稳定性及其质量控制标准等研究资料;
(四)新原料安全评估资料。
4、化妆品注册申请人、备案人应当具备下列条件:
(一)是依法设立的企业或者其他组织;
(二)有与申请注册、进行备案的产品相适应的质量管理体系;
(三)有化妆品不良反应监测与评价能力。
5、化妆品注册/备案提交资料清单:
(一)---(七)略,(八)产品安全评估资料
首次注册/备案需提交注册/备案人条件资料
进口:生产国上市证明或针对中国消费者研究试验资料(专供中国)、境外生产企业符合化妆品生产质量管理规范的证明资料
6、化妆品新原料和化妆品注册、备案前,注册申请人、备案人应当自行或者委托专业机构开展安全评估。
从事安全评估的人员应当具备化妆品质量安全相关专业知识,并具有5年以上相关专业从业经历。
7、化妆品的功效宣称应当有充分的科学依据。
化妆品注册人、备案人应当在国务院药品监督管理部门规定的专门网站公布功效宣称所依据的文献资料、研究数据或者产品功效评价资料的摘要,接受社会监督。
8、注册人、备案人、受托生产企业应:
需建立原料、内包材的进货查验记录制度、产品销售记录制度
进货查验记录和产品销售记录应当真实、完整,保证可追溯,保存期限(N≥1:N+1, N<1:≥2 )---其中N为产品有效期
需设质量安全负责人(质量安全、产品放行),条件:质量安全相关专业知识,5年以上化妆品生产或质量管理经验
建立人员健康管理制度:患有国务院卫生主管部门规定的有碍化妆品质量安全疾病的人员不得直接从事化妆品生产活动
定期自查质量管理体系(内审)(重大问题:立即整改;质量安全:停止生产,上报药监部门)
9、对经营过程的监管要求
经营者(包含专业线、酒店):
建立进货查验记录制度、产品销售记录制度,记录要真实、完整、可追溯,保存期限(N≥1:N+1, N<1:≥2 )---其中N为产品有效期
按法规、标签要求存储、运输化妆品,定期检查变质或过期情况
集中交易市场/展销会举办者:
查入场经营者:市场主体登记证明等
对入场经营者实施管理责任(NG: 上报药监部门)
电商平台:
对经营者实名登记,经营者要全面真实准确及时提供化妆品信息
对经营者实施管理责任(NG: 停止销售,上报药监部门)
10、违法事实描述与违法代价更加明确,企业依法生产经营的方向更清晰,执法部门监督处罚更有依据。
部分严重违法行为可能会被追究刑事责任。
举例如下:
条例第59条 违法事实:
无生产许可,受委托企业无生产许可证,生产经营或者进口未经注册的特殊化妆品,使用了禁用原料,或未注册新原料,或可能危害健康的有害物质,或过期原料等
违法代价:
没收非法所得、化妆品、原料、内包材
化妆品货值1万以内,罚款:5万-15万,化妆品货值1万以上,罚款:15N-30N (N为化妆品货值)
情节严重:
责令停产,取消备案,吊销许可证
10年内不能申请许可证或备案
法人、主要负责人、直接负责主管、其他直接责任人:罚款3N-5N (N为上一年度从本单位收入),终生禁止从事本业,可能会有刑事责任。
条例第60条 违法事实:
使用了不合格原料、内包材,或未备案新原料,或限用原料,生产经营不符合强制性国家标准、技术规范或者不符合化妆品注册、备案资料载明的技术要求的化妆品,未按照化妆品生产质量管理规范的要求组织生产,改产品有效期,经营者配制化妆品或销售变质、过期化妆品,拒不召回、拒不停产/停售等
违法代价:
没收非法所得、化妆品、原料、内包材
化妆品货值1万以内,罚款:1万-3万,化妆品货值1万以上,罚款:5N-20N (N为化妆品货值)
情节严重:
责令停产,取消备案,吊销许可证
法人、主要负责人、直接负责主管、其他直接责任人:罚款1N-3N (N为上一年度从本单位收入),10年禁止从事本业,可能会有刑事责任。
以上是2020新版《化妆品监督管理条例》的10大要点解读。
为了助力化妆品企业能快速的轻松应对新条例,SGS已于8月成功举办了主题为——新版《化妆品监督管理条例》条款要点解读的在线直播活动,老师在线重点分享了新版《化妆品监督管理条例》内容及新、旧化妆品监督条例对比,使在线学员对新版《化妆品监督管理条例》的重要变化及关键点有了更清晰的了解,对后续开展工作有了参考方向。
错过直播的小伙伴,扫描海报二维码即可观看回放!

SGS作为国际公认的检验、鉴定、测试和认证机构,是公认的质量和诚信的全球基准。在化妆品领域,可以为企业提供:
化妆品国际标准认证服务(ISO 22716; Cosmetic GMP ;EFfCI;ASEAN Cosmetic GMP)及相关各类培训等。

新条例10个关键点,涉及以下5个方面:
化妆品定义
化妆品和化妆品原料分类管理
安全评估和功效宣称
生产经营过程的要求
违法事实及代价
SGS专家针对新条例10个关键点的详细解析:
1、新条例中对化妆品定义:
指以涂擦、喷洒或者其他类似方法,施用于皮肤、毛发、指甲、口唇等人体表面,以清洁、保护、美化、修饰为目的的日用化学工业产品。
2、化妆品分类管理
化妆品分为特殊化妆品和普通化妆品。国家对特殊化妆品实行注册管理,对普通化妆品实行备案管理。
特殊:染发、烫发、祛斑美白、防晒、防脱发、宣称新功效---注册后,才能生产、进口
普通:其他---备案管理(国产:备案后上市;进口:备案后进口)
牙膏参照本条例有关普通化妆品的规定进行管理。牙膏的具体管理办法由国务院药品监督管理部门拟订,报国务院市场监督管理部门审核、发布。香皂不适用本条例,但是宣称具有特殊化妆品功效的适用本条例。
对本条例施行前已经注册的用于育发、脱毛、美乳、健美、除臭的化妆品自本条例施行之日起设置5年的过渡期,过渡期内可以继续生产、进口、销售,过渡期满后不得生产、进口、销售该化妆品。
3、化妆品原料分为新原料和已使用的原料。国家对风险程度较高的化妆品新原料实行注册管理,对其他化妆品新原料实行备案管理。
化妆品新原料:在我国境内首次使用于化妆品的天然或者人工原料为化妆品新原料。
特殊新原料:防腐、防晒、着色、染发、祛斑美白---注册管理
其他新原料:其他---备案管理
新原料转化为已用使用原料过程:
注册人/备案人3年内每年向国务院药监部门报告使用情况与安全性(YES: 纳入已用原料;NO: 撤销注册/取消备案)
申请化妆品新原料注册或者进行化妆品新原料备案,应当提交下列资料:
(一)注册申请人、备案人的名称、地址、联系方式;
(二)新原料研制报告;
(三)新原料的制备工艺、稳定性及其质量控制标准等研究资料;
(四)新原料安全评估资料。
4、化妆品注册申请人、备案人应当具备下列条件:
(一)是依法设立的企业或者其他组织;
(二)有与申请注册、进行备案的产品相适应的质量管理体系;
(三)有化妆品不良反应监测与评价能力。
5、化妆品注册/备案提交资料清单:
(一)---(七)略,(八)产品安全评估资料
首次注册/备案需提交注册/备案人条件资料
进口:生产国上市证明或针对中国消费者研究试验资料(专供中国)、境外生产企业符合化妆品生产质量管理规范的证明资料
6、化妆品新原料和化妆品注册、备案前,注册申请人、备案人应当自行或者委托专业机构开展安全评估。
从事安全评估的人员应当具备化妆品质量安全相关专业知识,并具有5年以上相关专业从业经历。
7、化妆品的功效宣称应当有充分的科学依据。
化妆品注册人、备案人应当在国务院药品监督管理部门规定的专门网站公布功效宣称所依据的文献资料、研究数据或者产品功效评价资料的摘要,接受社会监督。
8、注册人、备案人、受托生产企业应:
需建立原料、内包材的进货查验记录制度、产品销售记录制度
进货查验记录和产品销售记录应当真实、完整,保证可追溯,保存期限(N≥1:N+1, N<1:≥2 )---其中N为产品有效期
需设质量安全负责人(质量安全、产品放行),条件:质量安全相关专业知识,5年以上化妆品生产或质量管理经验
建立人员健康管理制度:患有国务院卫生主管部门规定的有碍化妆品质量安全疾病的人员不得直接从事化妆品生产活动
定期自查质量管理体系(内审)(重大问题:立即整改;质量安全:停止生产,上报药监部门)
9、对经营过程的监管要求
经营者(包含专业线、酒店):
建立进货查验记录制度、产品销售记录制度,记录要真实、完整、可追溯,保存期限(N≥1:N+1, N<1:≥2 )---其中N为产品有效期
按法规、标签要求存储、运输化妆品,定期检查变质或过期情况
集中交易市场/展销会举办者:
查入场经营者:市场主体登记证明等
对入场经营者实施管理责任(NG: 上报药监部门)
电商平台:
对经营者实名登记,经营者要全面真实准确及时提供化妆品信息
对经营者实施管理责任(NG: 停止销售,上报药监部门)
10、违法事实描述与违法代价更加明确,企业依法生产经营的方向更清晰,执法部门监督处罚更有依据。
部分严重违法行为可能会被追究刑事责任。
举例如下:
条例第59条 违法事实:
无生产许可,受委托企业无生产许可证,生产经营或者进口未经注册的特殊化妆品,使用了禁用原料,或未注册新原料,或可能危害健康的有害物质,或过期原料等
违法代价:
没收非法所得、化妆品、原料、内包材
化妆品货值1万以内,罚款:5万-15万,化妆品货值1万以上,罚款:15N-30N (N为化妆品货值)
情节严重:
责令停产,取消备案,吊销许可证
10年内不能申请许可证或备案
法人、主要负责人、直接负责主管、其他直接责任人:罚款3N-5N (N为上一年度从本单位收入),终生禁止从事本业,可能会有刑事责任。
条例第60条 违法事实:
使用了不合格原料、内包材,或未备案新原料,或限用原料,生产经营不符合强制性国家标准、技术规范或者不符合化妆品注册、备案资料载明的技术要求的化妆品,未按照化妆品生产质量管理规范的要求组织生产,改产品有效期,经营者配制化妆品或销售变质、过期化妆品,拒不召回、拒不停产/停售等
违法代价:
没收非法所得、化妆品、原料、内包材
化妆品货值1万以内,罚款:1万-3万,化妆品货值1万以上,罚款:5N-20N (N为化妆品货值)
情节严重:
责令停产,取消备案,吊销许可证
法人、主要负责人、直接负责主管、其他直接责任人:罚款1N-3N (N为上一年度从本单位收入),10年禁止从事本业,可能会有刑事责任。
以上是2020新版《化妆品监督管理条例》的10大要点解读。
为了助力化妆品企业能快速的轻松应对新条例,SGS已于8月成功举办了主题为——新版《化妆品监督管理条例》条款要点解读的在线直播活动,老师在线重点分享了新版《化妆品监督管理条例》内容及新、旧化妆品监督条例对比,使在线学员对新版《化妆品监督管理条例》的重要变化及关键点有了更清晰的了解,对后续开展工作有了参考方向。
错过直播的小伙伴,扫描海报二维码即可观看回放!

SGS作为国际公认的检验、鉴定、测试和认证机构,是公认的质量和诚信的全球基准。在化妆品领域,可以为企业提供:
化妆品国际标准认证服务(ISO 22716; Cosmetic GMP ;EFfCI;ASEAN Cosmetic GMP)及相关各类培训等。
16th Floor, Block A, No.73 Fucheng Road, Century Yuhui Mansion,
北京, Haidian District, 中国大陆



